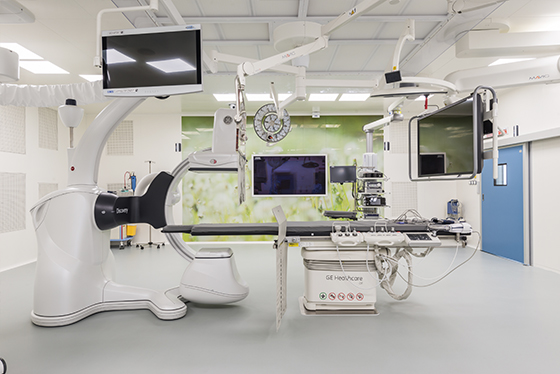
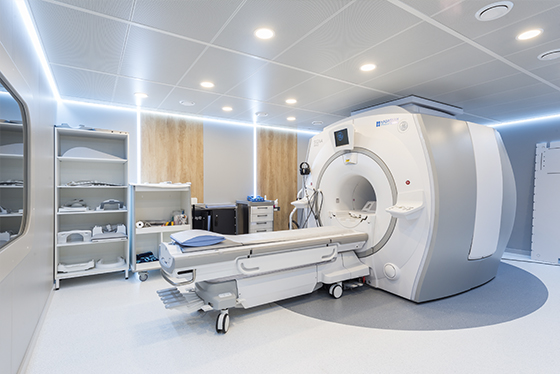
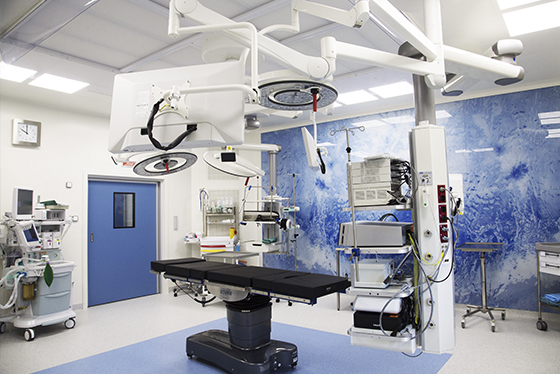
Международный медицинский центр Hadassah специализируется на лечении онкологических заболеваний. Для этого в наших стенах собраны все ресурсы: передовое оснащение центра хирургии и отделения лучевой терапии, международные протоколы лечения и препараты, недоступные для других медучреждений страны, и, конечно – талантливые, опытные врачи, в том числе специалисты из Израиля. Центр маммологии Hadassah предоставляет возможность женщинам в одном месте не только всестороннее обследовать молочную железу, но и пройти эффективное лечение рака молочной железы по израильским протоколам.
Команда специалистов Hadassah Medical Moscow работает вместе, чтобы обеспечить пациенту наилучшее лечение и уход. Мы подбираем лечение индивидуально для каждой женщины, учитывая стадию и степень рака, общее состояние здоровья, пережила ли пациентка менопаузу. Основными методами лечения рака молочной железы, которые применяются в международном медицинском центре Hadassah в Сколково являются: операция, лучевая терапия, химиотерапия, гормональная терапия, таргетная терапия. Лечащий врач может предложить пациенту один из этих методов лечения или их комбинацию. Их тип или комбинация будут зависеть от того, как был диагностирован рак и на какой стадии он находится. Лечащий врач всегда подробно обсуждает с пациентом наиболее подходящие методы лечения, предстоящие этапы подготовки, лечения и восстановления, а также перспективы лечения рака молочной железы в нашей клинике.
Рак молочной железы (РМЖ) – достаточно агрессивная опухоль, которая является результатом бесконтрольного роста злокачественных клеток. На фоне интоксикации организма, характерной для раковых процессов, происходит развитие опасных сопутствующих заболеваний.
Речь идет о самой распространенной онкологической патологииу женщин. Каждый год в России диагностируется около 55 тыс. случаев заболевания (на долю мужчин приходится менее 1%).
ОСОБЕННОСТИ ЛЕЧЕНИ РАКА МОЛОЧНО ЖЕЛЕЗЫ В КЛИНИКЕ HADASSAH MEDICAL MOSCOW
ОТЗЫВЫ ПАЦИЕНТОВ
Симптомы рака груди
Рак груди имеет системный характер развития болезни. Происходит не только непосредственное поражение ткани, но и разрушительное воздействие злокачественного образования на сам организм. Поэтому развитие болезни может сопровождаться проявлением общих симптомов.

Как и другие онкологические заболевания, на начальных стадиях РМЖ в основном протекает бессимптомно. Поэтому, пока патология не перешла в запущенную стадию, следует с особым вниманием относиться к своему здоровью.
Поводом для посещения врача являются следующие симптомы:
- любое уплотнение в груди;
- выделения из сосков (прозрачные или кровянистые);
- втяжение соска или изменение формы;
- появление участков с втянутой кожей;
- покраснение кожного покрова;
- появление отеков, морщин;
- изменение формы груди, соска или ареола.
Метастазы при раке молочной железы распространяются по организму через кровь и лимфатическую систему. Происходит поражение подмышечных, надключичных и подключичных лимфоузлов, поэтому при движении рукой со стороны опухоли возникает болевой синдром. На сильно запущенных стадиях на коже груди появляются незаживающие язвочки.
ВИДЕО ЭКСПЕРТОВ ЦЕНТРА
Постановка диагноза при РМЖ
Мы уделяем большое внимание рождению детей и семье, поэтому женское здоровье для нас в приоритете. Каждая женщина, обратившаяся в клинику, имеет возможность пройти полный комплекс обследования груди на современных аппаратах с высокой степенью детализации в кратчайшие сроки. Такой подход избавляет женщину от необходимости посещения множества специалистов, длительного ожидания результата биопсии, так как гистологическое заключение в нашей клинике будет готово за сутки. На первом визите, после осмотра мы можем провести весь спектр необходимых обследований, а именно маммографию, УЗИ, МРТ, а также выполнить все виды биопсии. Цитологическое заключение пациентка сможет получить в течение 1-2 часов, а гистологический анализ – в течение суток. Возможность применения всех самых современных методов обследования (включая генетическую и радиоизотопную диагностику, томосинтез, МРТ с контрастированием) в нашем центре в день первичного обращения играет ключевую роль при подозрении на злокачественный процесс. После нескольких дней обследования специалист международной команды клиники разрабатывает индивидуальную схему лечения, максимально эффективную для каждой пациентки.
Хирургия рака молочной железы
Хирурги-маммологи клиники имеют многолетнюю практику проведения хирургического лечения рака молочной железы, выполняя множество операций:
Лучевая терапия
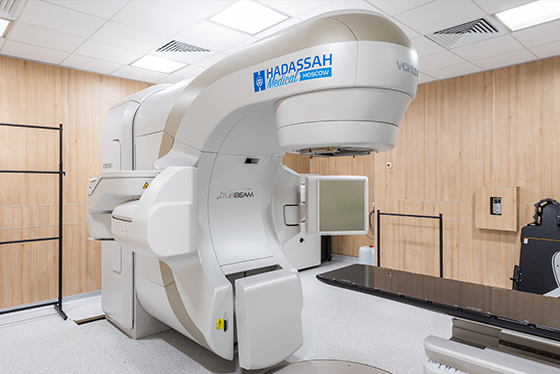
Послеоперационная лучевая терапия при раке молочной железы проводится в клинике Hadassah Moscow по уникальной методике, с применением передовых технологий дозиметрического планирования и проведения сеансов на линейных ускорителях Varian TrueBeam STX, имеющих специальные опции для лучевой терапии с синхронизацией по дыханию. Лучевая терапия использует контролируемые дозы радиации для уничтожения раковых клеток. Обычно его назначают после операции и химиотерапии, чтобы убить все оставшиеся раковые клетки.
Подробнее о лучевой терапии молочной железы.
Химиотерапия
Химиотерапия при раке молочной железы является важной частью лечения помимо операции, облучения и гормональной терапии. Лечение химиотерапевтическими препаратами обычно включает внутривенное введение и пероральный прием. Будет ли использован данный метод, зависит от индивидуальной ситуации: химиотерапия до или после операции может снизить риск рецидива. У женщин с прогрессирующим заболеванием прием цитостатиков может замедлить рост опухоли.
В медицинском центре Hadassah в лечении данного заболевания применяются схемы лечения, утвержденных международными рекомендациями. Количество курсов определяется индивидуально на основании действующих клинических рекомендаций международного уровня. Химиотерапию при раке молочной железы можно проводить как стационарно, так и амбулаторно, сохраняя при этом трудоспособность пациентки.
ГОРМОНАЛЬНАЯ ТЕРАПИЯ
Гормональная терапия, также называемая эндокринной терапией, является эффективным средством при раке молочной железы. Блокирование гормонов, при самостоятельном применении или после химиотерапии, поможет предотвратить рецидив рака и смерть от онкологии. Гормональная терапия может назначаться перед операцией, для уменьшения опухолей, облегчения хирургического вмешательства и снижения риска рецидива и называться неоадъювантной гормональной терапией. Кроме того, она может назначаться после хирургического вмешательства для снижения риска рецидива, тогда это называется адъювантной гормональной терапией.
ИММУНОТЕРАПИЯ
Иммунотерапия, также называемая биологической терапией, предназначена для повышения естественной защиты организма от онкологии. В ней используются вещества, вырабатываемые организмом или произведенные в лаборатории для улучшения, направления или восстановления функции иммунной системы.
Опытные онкологи высшей категории московского филиала израильской клиники Hadassah занимаются лечением заболевания рак молочной железы не только у московских пациентов, но и жителей других регионов: Санкт-Петербурга, Нижнего Новгорода, Екатеринбурга, Краснодара, Новосибирска и других.
ТАРГЕТНАЯ ТЕРАПИЯ
Таргетная терапия — лечение, направленное на специфические гены, белки или тканевую среду рака, способствующую росту и выживанию рака. Этот тип лечения блокирует рост и распространение раковых клеток, одновременно ограничивая повреждение здоровых клеток.
Не все опухоли имеют одинаковые мишени. Чтобы найти наиболее эффективное лечение, ваш врач может провести анализы для определения генов, белков и других факторов вашей опухоли. Кроме того, научные исследования позволяют узнавать больше о конкретных молекулярных мишенях и новых методах лечения, направленных на них.
Источники
Пак Д., Рассказова Е. Рак молочной железы //Врач. – 2005. – №. 12. – С. 3-8.
Семиглазов В. Ф., Семиглазов В. В., Дашян Д. Скрининг рака молочной железы //Практическая онкология. – 2010. – Т. 11. – №. 2. – С. 60-65.
Летягин В. П., Высоцкая И. В., Ким Е. А. Факторы риска развития рака молочной железы //Опухоли женской репродуктивной системы. – 2006. – №. 4. – С. 10-12.
Жукова Л. Г. и др. Рак молочной железы //Современная онкология. – 2021. – Т. 23. – №. 1. – С. 5-40.
Имянитов Е. Н. и др. Наследственный рак молочной железы //Практическая онкология. – 2010. – Т. 11. – №. 4. – С. 258-266.